Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (34): 5547-5552.doi: 10.3969/j.issn.2095-4344.0639
Previous Articles Next Articles
Application of nano-hydroxylapatite/collagen and its mineralized composites in bone tissue engineering
Zhang Xue, Zhang Yang
- Stomatological Hospital of China Medical University, Shenyang 110002, Liaoning Province, China
-
Received:2018-06-01Online:2018-12-08Published:2018-12-08 -
About author:Zhang Xue, MD, Lecturer, Attending physician, Stomatological Hospital of China Medical University, Shenyang 110002, Liaoning Province, China
CLC Number:
Cite this article
Zhang Xue, Zhang Yang. Application of nano-hydroxylapatite/collagen and its mineralized composites in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(34): 5547-5552.
share this article
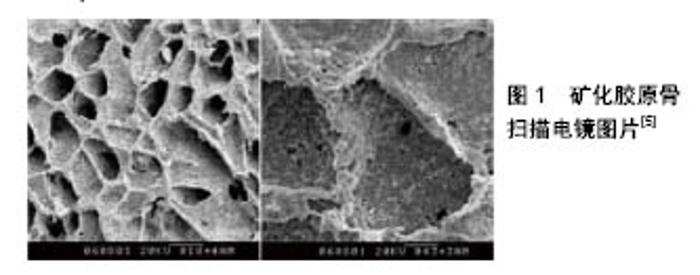
2.1 矿化胶原骨理化性能 2.1.1 三维框架 骨组织属于胶原-磷酸钙复合系统,其主要组成是水,有机物和无机盐等,是一个复杂的天然生物矿化系统。天然骨中矿物占70%左右,Ⅰ型胶原是骨中最主要的结构蛋白,它占有骨干质量的30%,而且是骨中非矿物相成分的90%-95%[15],其余成分为少量有机物。骨的组合即是通过将磷酸钙矿物有序地沉积在胶原基质上,再将矿化的胶原有序排列而成。 矿化胶原骨为一种新型的骨组织工程支架材料,其基础成分为具有碳酸根的羟基磷灰石与胶原,为纳米量级的晶体尺寸[16]。矿化胶原骨具有多孔的三维构造,与天然松质骨相似,该材料具有孔隙率为80%,孔径介于50- 300 μm之间,基材及结构与天然骨极为相似,见图1[5]。"
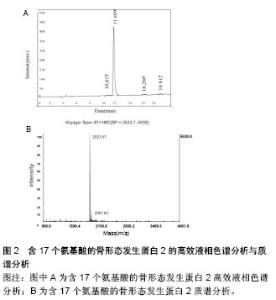
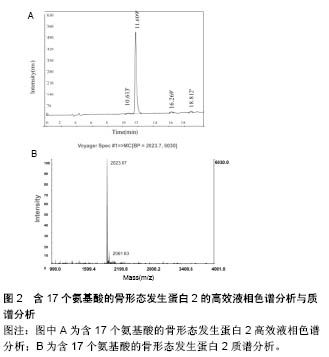
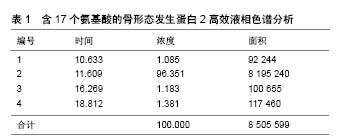
作为支架材料,孔径大于100 μm,有利于承载细胞的黏附、生长和增殖;孔径小于50 μm,可为细胞代谢活动提供有利条件[17]。张丽军等[18]在研究中发现,骨缺损周边有纤维组织长入矿化胶原多孔框架,成骨细胞位于新生骨小梁周围,在新生骨组织、宿主骨周围可见与材料骨性结合的现象,证明了新骨形成,以及支架材料良好的骨相容性、诱导成骨性能及可降解性。矿化胶原骨在材料的诱导下,新生的纤维细胞可在框架中穿插生长,并为钙盐沉积提供基础。同时材料的多孔结构使细胞易于长入,与细胞具有良好的亲和性,细胞易于贴壁、增殖、迁移,同时营养物质也便于运输[19]。 2.1.2 生物相容性 生物材料应该具有良好的生物相容性,整合到宿主的组织中而不引起免疫排斥反应,符合生物安全评价的标准,这是应用于临床的基础和前提。作为骨缺损的修复材料,许多学者对矿化胶原骨的生物相容性进行了研究,研究表明其具有优良的生物相容性[20]。在体外实验中,王明海等[21]发现矿化胶原骨可为兔骨髓基质干细胞的黏附、代谢增殖提供条件,矿化胶原骨表面骨髓基质干细胞的活性和碱性磷酸酶活性与对照组无统计学差异。有学者将矿化胶原骨与骨髓间充质干细胞复合培养,发现骨髓间充质干细胞可在矿化胶原骨上黏附、生长、繁殖、分化,复合前后表型一致,证实其具有良好的生物相容性[22]。 2.1.3 生物可降解性 降解是物质分子量变小的化学反应总称,其中包括分子链的解聚、无规则断链、侧基和低分子物的脱除等反应[23]。生物降解通常是指在分泌酶的微生物(细菌、真菌)作用下,导致材料分子量降低的过程。对于医用生物降解材料而言,是指在生物体的体液、酶、细胞等多种因素综合作用下,逐步减小生物材料的分子量。在可降解材料的研究中,材料的降解速率及降解之后小分子产物的生物安全性是值得关注的问题。 组织工程骨的支架材料应具有良好的生物降解性能,同时降解速率最好与新生骨的生成率尽可能接近,从而维持骨的高度和宽度,这对口腔种植手术尤为重要。以往骨替代材料的研究发现,晶体尺寸较大的羟基磷灰石支架材料,破骨细胞无法有效降解、吸收替代,即使延长植入时间也无法获得满意的结果。而纳米级矿化胶原骨晶体具有比表面积大的特点,很容易被机体降解、吸收,同时,其降解产物不改变周围环境的pH值,降解过程模拟天然骨的新陈代谢,降解产物不会改变机体局部环境,降解速率与成骨具有良好的匹配,有效修复骨缺损[24]。有学者在实验中观察到支架材料界面层有活跃的溶解-再沉积过程,这与缺损再生修复早期形成的具有不断更新和成熟活动特色的网状骨生理活动很相似[8]。同时,矿化胶原骨的基础三维框架结构及尺寸大小是使材料表面发生快速更新的关键因素。 2.1.4 成骨活性 矿化胶原骨具有良好的骨传导性能,在骨组织工程研究中已得到了充分的肯定[25]。有研究指出生物材料植入缺损部位促进新骨形成,与材料表面是否形成类骨磷灰石层及富Ca-P层关系密切,进而关系到生物活性陶瓷等骨组织工程材料是否能形成骨结合与骨形成[26]。矿化胶原骨在模拟天然骨的成分和结构特征的基础上,具有纳米量级尺寸、低结晶度,是含碳酸根和胶原的羟基磷灰石矿物基材,该材料具有与骨结合的能力,为胶原和矿物的沉积提供承载条件,可为成骨细胞黏附提供有利环境,便于其植入,促进骨生长[8,27]。 2.2 矿化胶原骨复合材料的应用 骨组织工程有3大要素,其中框架材料作为载体,提供新骨形成的支架,可为缺损位置运送生物活性分子。而骨诱导因子作用的目标细胞是具有多向分化潜能的间充质干细胞,通常位于血管周围,在骨诱导因子的作用下,一方面可诱导间充质干细胞分化为软骨细胞、骨细胞,可在修复大面积缺损中担任重要的角色;另一方面,骨诱导因子“诱导成骨”参与新骨形成的过程,即通过刺激成骨性细胞的有丝分裂,进而促进新骨产生。骨缺损的组织修复是多方面因素协调作用的复杂过程,3个关键要素在骨组织修复中相辅相成。以往研究表明,由于骨替代材料没有骨诱导因子、干细胞等生物活性物质,其成骨效果仍不如自体骨[6]。因此,矿化胶原骨的临床应用受到了一定程度的限制。但矿化胶原骨具有良好的复合性,同时可作为优良的生物活性物质载体,矿化胶原骨复合材料在骨组织工程研究中得到了充分肯定并具有良好的应用前景。 2.2.1 矿化胶原骨复合天然骨材料 自体骨为良好的移植材料,不但能够保持细胞活性,而且骨基质中富含成骨诱导的细胞因子,可刺激骨母细胞分化,促进新骨形成。但是获取自体骨最大的弊端是,造成患者的心理负担与痛苦,加大患者创伤,增加手术难度和时间成本,取骨部位术后疼痛等缺陷,大面积缺损还会存在骨源不足等困扰。随后学者开始关注异种移植材料,其具有容易获取的优势,但植入后不可避免会导致机体免疫排斥反应的发生,致移植失败。去除牛骨内有机成分的Bio-Oss骨粉植入人体内虽然不会发生免疫排斥反应[28],但Bio-Oss骨粉的缺点是降解缓慢,有报道指出种植后9年仍能检测到未吸收的骨粉[29]。经处理后的珊瑚人工骨具有良好的生物相容性和骨亲和性,但珊瑚人工骨质地脆、吸收快,植入后有一定的体积变化。联合应用矿化胶原骨和天然骨材料,避免了异位取骨的二次手术创伤,操作简便易行,又减少天然骨材料的用量,为临床植骨提供了充足的替代骨源。沈铁城等[6]指出在骨科疾病的临床应用中,矿化胶原骨具有良好的生物相容性、生物可降解性,植入体内有良好的骨传导作用,但因其不具备骨诱导成分,对于骨不连、两性骨肿瘤等所致的骨缺损,宜将矿化胶原骨与自体骨混合使用。 2.2.2 矿化胶原骨复合人工骨材料 利用矿化胶原骨 复合人工骨材料可在一定程度上发挥矿化胶原骨及其他人工骨材料各自的优势,达到更加有效修复骨组织缺损的目的。Liu等[30-31]将不同配比的矿化胶原骨和半水硫酸钙制备矿化胶原骨/半水硫酸钙复合水泥,研究其凝固时间、机械性能、体外生物活性和降解性、体外及体内生物相容性、体内成骨性能等,结果证明与纯半水硫酸钙相比,矿化胶原骨/半水硫酸钙复合水泥有更好的生物相容性及较强的骨改建能力。张超等[17]将矿化胶原骨与聚乳酸复合制成矿化胶原骨-聚乳酸三维框架,通过实验证明该支架可作为骨组织工程良好的细胞外基质材料。同时,有文献报道矿化胶原骨/聚乳酸具有良好的生物相容性,组织学分析发现与羟基磷灰石/磷酸三钙相比明显促进了新骨形成[32]。有学者在研究中将藻酸盐钙水凝胶和矿化胶原骨复合,证明此新型可注射复合材料具有良好的机械性能和生物活性[33]。朱超等[34]制备的液态羟基磷灰石胶原海藻酸钠复合材料,具有微创、恢复快等优点,达到促进骨愈合的作用。 2.2.3 矿化胶原骨复合细胞及血浆 在没有框架材料支持情况下的细胞植入,机体无法有效利用,植入局部的细胞无法定植,同时不能达到有效诱导成骨所需的细胞数量,这是导致骨缺损修复效果不尽如人意的主要原因。矿化胶原骨这种良好的骨组织工程支架材料,可为植入的细胞提供黏附及生长繁殖的条件,促进局部骨形成与骨再生。李冬梅等[35]将纳米晶胶原骨材料(矿化胶原骨)与山羊骨髓间充质干细胞体外复合培养,发现细胞在材料上能够良好地黏附和生长,在兔下颌缺损实验中发现复合材料组比单独应用矿化胶原骨具有较好的骨再生能力。孙伟等[25]用影像学方法观察纳米人工骨和骨髓间充质干细胞治疗股骨头坏死缺损动物模型的效果,指出加用骨髓间充质干细胞可促进骨缺损的修复,有利于骨组织再生。彭程等[36]实验证明复合后材料具有一定的骨诱导作用,注入体内后成骨速度、形成新骨质量及力学强度明显优于单纯的纳米骨浆或红骨髓,可用于经皮注射修复实验性骨不连。杨新明等[37]在实验中证明自体骨髓基质干细胞可很好地与支架材料复合,具有良好的成骨效果。现阶段,许多学者尝试将干细胞与支架复合用于治疗骨组织缺损,并取得了显著进展[27,35]。 2.2.4 矿化胶原骨复合生物因子及药物 骨组织修复过程需要多种因子的参与,是生物体在激素和局部生物活性因子的调控下,生物分子在生物体内的信息转导,是一个复杂的生物过程[38]。影响骨组织形成的因素有很多,比如激素(甲状旁腺素、甲状腺素等)、生物活性因子(骨形态发生蛋白、白细胞介素等)[39]。其中,生物活性因子在骨缺损修复过程中起着至关重要的作用。骨形态发生蛋白是骨组织工程中应用最多的生物活性因子[40-41]。其中,骨形态发生蛋白2是目前研究最为广泛、诱导成骨活性最强的骨形态发生蛋白之一。Han等[42]在矿化胶原骨复合材料应用于兔腰椎间盘横突间融合中发现,矿化胶原骨能够与骨形态发生蛋白2良好地复合,复合材料具有比矿化胶原骨更佳的降解及成骨性能。因为天然的骨形态发生蛋白2数量有限,目前国内外多采用基因工程学等技术制备基因重组人骨形态发生蛋白2,但人工合成的骨形态发生蛋白2 的制备工艺非常复杂,存在生产周期长、成本高、转染效率低、表达时间较短及病毒载体的潜在致癌性等缺点[43-44]。近年来的研究发现,骨形态发生蛋白2的生物效应是通过其分子抗原决定族与细胞膜上受体形成异聚复合物来实现的[45]。在此基础上,许多针对不同活性位点的骨形态发生蛋白2活性多肽应运而生,国内外对骨形态发生蛋白2活性多肽的研究也取得了新进展[46-48]。短链多肽可通过多肽合成仪大规模制备,降低了成本,提高了材料的安全性。同时,短链多肽上与细胞表面受体结合的活性位点能够充分暴露,具有更强的生物活性[49-50],其可增强材料的骨诱导性和生物相容性,为矿化胶原骨/骨形态发生蛋白2活性多肽复合物的开发及应用创造条件。有学者证实P24活性多肽具有体外定向诱导大鼠骨髓间充质干细胞向成骨方向定向分化的作用,且这种诱导作用具有剂量依赖性[50], 高分子聚合材料复合该多肽后具有骨诱导活性,成骨能力增强[32]。清华大学材料教研室崔福斋团队以骨形态发生蛋白2的32-48功能区为模板,自主设计合成含17个氨基酸的具有骨诱导活性的蛋白多肽(P17-BMP-2,IVAPPGYHAFYCHGECP),其纯度为96%,平均分子量为2 023.67 m/z(表1,图2),将其与矿化胶原骨复合制成新短肽P17-骨形态发生蛋白2/矿化胶原骨材料,进一步提高了矿化胶原骨的生物相容性,改善了矿化胶原骨的骨诱导性,增强了其修复骨缺损的能力 [48]。 2.2.5 矿化胶原骨复合多种生物活性物质 为了进一步提高成骨性能,越来越多的学者制备矿化胶原骨复合多种生物活性物质的骨组织工程材料[51-53]。Patel等[54]尝试观察了在血管内皮生长因子和骨形态发生蛋白2双重作用下矿化胶原骨对于鼠颅骨临界缺损模型骨再生的影响,发现骨再生作用得到了一定程度的增强。有学者将组织工程支架(矿化胶原骨/PLLA/CMs)复合骨形态发生蛋白2合成肽,经实验证明该支架具有良好的机械性能,并能诱导增强骨髓基质干细胞的碱性磷酸酶活 性[55]。有报道显示壳聚糖聚乳酸羟基乙酸纳米羟基磷灰石支架具有良好的生物形容性及成骨诱导性,复合重组人骨形态发生蛋白2或其合成肽(P24)在鼠颅骨缺损模型中显示了有效的骨损伤修复能力[56]。张广德等[57]探讨腺病毒介导骨形态发生蛋白9/EPO双基因共转染脂肪干细胞复合矿化胶原骨/聚乳酸支架材料促进体内成骨的可行性,实验证明其可显著促进下颌骨缺损的修复。 "
| [1] Jorgenson SS,Lowe TG,France J,et al.A prospective analysis of autograft versus allograft in posterolateral lumbar fusion in the same patient. A minimum of 1-year follow-up in 144 patients.Spine(Phila Pa 1976).1994;19(18):2048-2053.[2] Samartzis D,Shen FH,Matthews DK,et al.Comparison of allograft to autograft in multilevel anterior cervical discectomy and fusion with rigid plate fixation.Spine J.2003;3(6):451-459.[3] Thalgott JS,Fritts K,Giuffre JM,et al.Anterior interbody fusion of the cervical spine with coralline hydroxyapatite.Spine(Phila Pa 1976). 1999;24(13):1295-1299.[4] Tsuruga E,Takita H,Itoh H,et al.Pore size of porous hydroxyapatite as the cell-substratum controls BMP-induced osteogenesis.J Biochem. l997;121(3):317-324.[5] 崔福斋.组织工程的发展趋势[J].中国医疗器械信息, 2010,16(2):16-21.[6] 沈铁城,夏青,黄永辉,等.纳米晶胶原基骨材料在骨科疾病中的应用[J].中国组织工程研究与临床康复,2007,11(1): 48-51.[7] 俞兴,徐林,崔福斋.纳米晶胶原基骨材料在颈椎前路中的临床应用[J].生物骨材料与临床研究,2003,1(1):14-16.[8] 冯庆玲,崔福斋,张伟.纳米羟基磷灰石/胶原骨修复材料[J].中国医学科学院学报,2002,24(2):124-128.[9] 俞兴,崔福斋. 移植替代材料在脊柱外科中的应用[J].生物骨科材料与临床研究,2004,1(4):52-54.[10] Stock UA,Vacanti JP.Tissue engineering: current state and prospects. Ann Rev Med.2001;52:443-451.[11] Du C,Cui FZ,Feng QL,et al.Tissue response to nano-hydroxyapatite/ collagen composite implants in marrow cavity. J Biomed Mater Res. 1998;42(4):540-548.[12] Liao SS,Cui FZ,Zhang W,et al.Hierarchically biomimetic bone scaffold materials: nano-HA/collagen/PLA composite.J Biomed Mater Res B. 2004;69(2):158-165.[13] Huang Z,Tian J,Yu B,et al. A bone-like nano-hydroxyapatite/ collagen loaded injectable scaffold. Biomed Mater. 2009;4(5):055005. [14] Liu X,Li X,Fan Y,et al. Repairing goat tibia segmental bone defect using scaffold cultured with mesenchymal Stem Cells. 2010;94(1):44-52.[15] Scotchford CA,Cascone MG,Downes S,et al.Osteoblast responses to collagen-PVA bioartificial polymers in vitro: the effects of cross-linking method and collagen content. Biomaterials.1998;19(1-3):1-11.[16] Harris SE,Bonewald LF,Harris MA,et al.Effects of transforming growth factor beta on bone nodule formation and expression of bone morphogenetic protein 2, osteocalcin, osteopontin, alkaline phosphatase, and type I collagen mRNA in long-term cultures of fetal rat calvarial osteoblasts.J Bone Miner Res.1994;9(6):855-863.[17] 张超,胡蕴玉,张曙光,等.羟基磷灰石/胶原-聚乳酸三维多孔框架材料的制备成型及分析[J].中国生物医学工程学报, 2004,23(5):438-442.[18] 张丽军,王影,吴燕丽,等.胶原基纳米骨修复兔下颌骨缺损的实验研究[J].中国骨质疏松杂志,2004,10(2):155-157.[19] Sachlos E,Gotora D,Czernuszka JT.Collagen scaffolds reinforced with biomimetic composite nano-sized carbonate-substituted hydroxyapatite crystals and shaped by rapid prototyping to contain internal microchannels.Tissue Eng.2006;12(9):2479-2487.[20] He H,Yu J,Cao J,et al.Biocompatibility and Osteogenic Capacity of Periodontal Ligament Stem Cells on nHAC/PLA and HA/TCP Scaffolds. J Biomater Sci.2011;22:179-194.[21] 王明海,董有海,冯庆玲,等.纳米组织工程骨与兔骨髓基质干细胞体外生物相容性的实验研究[J].中国骨与关节损伤杂志, 2008,23(9):745-747.[22] 孙伟,李子荣,张岚,等.纳米晶胶原基骨与骨髓间充质干细胞复合培养对表型影响[J].中国误诊学杂志,2006,6(8):1419-1421.[23] 裴国献,魏宽海,金丹.组织工程学实验技术[M].北京:人民军医出版社, 2006.[24] Liao SS,Cui FZ.In vitro and in vivo degradation of mineralized collagen-based composite scaffold: nanohydroxyapatite/collagen/poly (L-lactide).Tissue Eng. 2004;10(1-2):73-80.[25] 孙伟,李子荣,史振才,等.纳米晶胶原基骨和骨髓间充质干细胞复合修复兔股骨头坏死缺损的研究[J].中国修复重建外科杂志, 2005,19(9):703-706.[26] Neo M,Nakamura T,Ohtsuki C,et al.Apatite formation on three kinds of bioactive material at an early stage in vivo: a comparative study by transmission electron microscopy.J Biomed Mater Res. 1993;27(8): 999-1006.[27] Liu HC,E LL,Wang DS,et al. Reconstruction of alveolar bone defects using bone morphogenetic protein 2 mediated rabbit dental pulp stem cells seeded on nano-hydroxyapatite/ collagen/poly (L-lactide).Tissue Eng Part A. 2011;17(19-20):2417-2433. [28] Stavropoulos A,Kostopoulos L,Nyengaard JR,et al.Fate of bone formed by guided tissue regeneration with or without grafting of Bio-Oss or Biogran. An experimental study in the rat.J Clin Periodontol.2004;31(1):30-39.[29] Traini T,Valentini P,Iezzi G,et al.A histologic and histomorphometric evaluation of anorganic bovine bone retrieved 9 years after a sinus augmentation procedure.J Periodontol.2007;78(5):955-961.[30] Liu HY,Liu X,Zhang LP,et al.Improvement on the performance of bone regeneration of calcium sulfatehemihydrate by adding mineralized collagen.Tissue Eng Part A. 2010;16(6):2075-2084.[31] Liu X,Wang XM,Chen Z,et al.Injectable bone cement based on mineralized collagen.J Biomed Mater Res B Appl Biomater. 2010; 94(1):72-79.[32] Li J,Hong J,Zheng Q,et al.Repair of rat cranial bone defects with nHAC/PLLA and BMP-2-related peptide or rhBMP-2.J Orthop Res. 2011;29(11):1745-1752.[33] Tan R,Niu X,Gan S,et al. Preparation and characterization of an injectable composite.J Mater Sci Mater Med. 2009;20(6):1245-1253.[34] 朱超,王华,刘伟,等.液态羟基磷灰石胶原海藻酸钠(Alg/nHAC)人工骨促进Ilizarov骨延长骨愈合的实验研究[J].生物骨科材料与临床研究, 2016, 13(6):5-9.[35] 李冬梅,刘新晖,李庆星.山羊颌骨骨髓间充质干细胞与纳米晶胶原骨材料体外复合培养[J].口腔医学研究,2018,34(1):22-26.[36] 彭程,崔福斋,朱振安,等.生物活性纳米骨浆复合自体红骨髓经皮注射修复实验性兔尺骨骨不连[J].中国组织工程研究与临床康复, 2010,14(21): 3801-3805.[37] 杨新明,石蔚,杜雅坤,等.浓集自体骨髓基质干细胞组织工程复合物治疗早期股骨头坏死的实验疗效[J].生物骨科材料与临床研究,2008,5(3):1-5.[38] Xu L,Lv K,Zhang W,et al.The healing of critical-size calvarial bone defects in rat with rhPDGF-BB, BMSCs, and β-TCP scaffolds.J Mater Sci Mater Med.2012;23(4):1073-1084. [39] 吕刚,梅晰凡,刘畅.医学干细胞实验技术[M].沈阳:辽宁科学技术出版社, 2010.[40] Chen D,Zhao M,Mundy GR.Bone morphogenetic proteins. Growth Factors.2004;22(4):233-241.[41] Costa JJ,Passos MJ,Leitão CC,et al.Levels of mRNA for bone morphogenetic proteins, their receptors and SMADs in goat ovarian follicles grown in vivo and in vitro.Reprod Fertil Dev. 2012;24(5):723-732. [42] Han DK,Kim CS,Jung UW,et al.Effect of a fibrin-fibronectin sealing system as a carrier for recombinant human bone morphogenetic protein-4 on bone formation in rat calvarial defects.J Periodontol.2005; 76(12):2216-2222.[43] Saito N,Takaoka K.New synthetic biodegradable polymers as bmp carriers for bone tissue engineering. Biomaterials. 2003;24(13): 2287-2293.[44] Griesenbach U,Geddes DM,Alton EW.Advances in cystic fibrosis gene therapy.Curr Opin Pulm Med. 2004;10(6):542-546.[45] Kirsch T,Sebald W,Dreyer MK.Crystal structure of the bmp-2-bria ectodomain complex.Nat Struct Biol. 2000;7(6):492-496.[46] 段智霞,郑启东,郭晓东,等 BMP2活性多肽/PLGA复合物植入异位成骨的实验研究[J].国际生物医学工程杂志,2007,30(3):129-132.[47] Saito A,Suzuki Y,Kitamura M,et al.Repair of 20-mm long rabbit radial bone defects using BMP-derived peptide combined with an alpha-tricalcium phosphate scaffold.J Biomed Mater Res A. 2006; 77(4):700-706.[48] Zhang X,Guo WG,Cui H,et al.In vitro and in vivo enhancement of osteogenic capacity in a synthetic BMP-2 derived peptide-coated mineralized collagen composite.J Tissue Eng Regen Med. 2016;10(2): 99-107.[49] Geiger M,Li RH,Friess W.Collagen sponges for bone regeneration with rhBMP-2.Adv Drug Deliv Rev. 2003;55(12):1613-1629.[50] 段智霞,郑启新,郭晓东,等.BMP-2活性多肽体外定向诱导大鼠BMSCs向成骨方向分化的实验研究[J].中华矫形外科杂志, 2007,15(21):1647-1650.[51] Jiang X,Zhong Y,Zheng L,et al.Nano-hydroxyapatite/collagen film as a favorable substrate to maintain the phenotype and promote the growth of chondrocytes cultured in vitro.Int J Mol Med.2018;41(4):2150-2158.[52] Wang X,Zhang G,Qi F,et al.Enhanced bone regeneration using an insulin-loaded nano-hydroxyapatite/collagen/PLGA composite scaffold. Int J Nanomedicine.2017;13:117-127.[53] 赵征,刘洪臣,黄征难,等.大鼠牙源性细胞复合nHAC/PLA支架体内构建牙体组织-骨复合体样结构的研究[J].口腔医学研究, 2016,32(3):244-248.[54] Patel ZS,Young S,Tabata Y,et al.Dual delivery of an angiogenic and an osteogenic growth factor for bone regeneration in a critical size defect model. Bone. 2008;43(5):931-940.[55] Niu X,Feng Q,Wang M,et al.Porous nano-HA/collagen/PLLA scaffold containing chitosan microspheres for controlled delivery of synthetic peptide derived from BMP-2.J Control Release.2009;134(2):111-117. [56] Ji Y,Wang M,Liu W,et al.Chitosan/nHAC/PLGA microsphere vehicle for sustained release of rhBMP-2 and its derived synthetic oligopeptide for bone regeneration.J Biomed Mater Res A.2017;105(6):1593-1606.[57] 张广德,靳霞,李荣亮,等.BMP-9/EPO 双基因共转染ADSCs复合nHAC/ PLA支架修复兔下颌骨缺损的实验研究[J].中国口腔颌面外科杂志,2017, 15(3):202-208.[58] Shen JY,Chan-Park MB,He B,et al.Three-dimensional microchannels in biodegradable polymeric films for control orientation and phenotype of vascular smooth muscle cells. Tissue Eng.2006;12(8):2229-2240. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||